疾病介绍|VEXAS 综合征
发布日期:2024-01-02
01
VEXAS 综合征分子致病机制
VEXAS综合征(液泡、E1酶、X -连锁、自身炎症、体细胞)是一种由造血祖细胞UBA1体细胞突变引起的成年型单基因疾病,由于影响编码E1泛素连接酶的UBA1基因蛋氨酸41发生体细胞的获得性突变,导致催化受损的同种型过表达,从而引发炎症反应。
02
VEXAS 综合征是如何发现的?
筛选了2560名患者(未确诊的复发性发热、全身性炎症或患有非典型未分类疾病,确定了3名男性,他们都存在一个新的杂合变异,是X-连锁的UBA1基因, (p.Met41), 该位点公共数据库中未收录,且预测有害的变异。
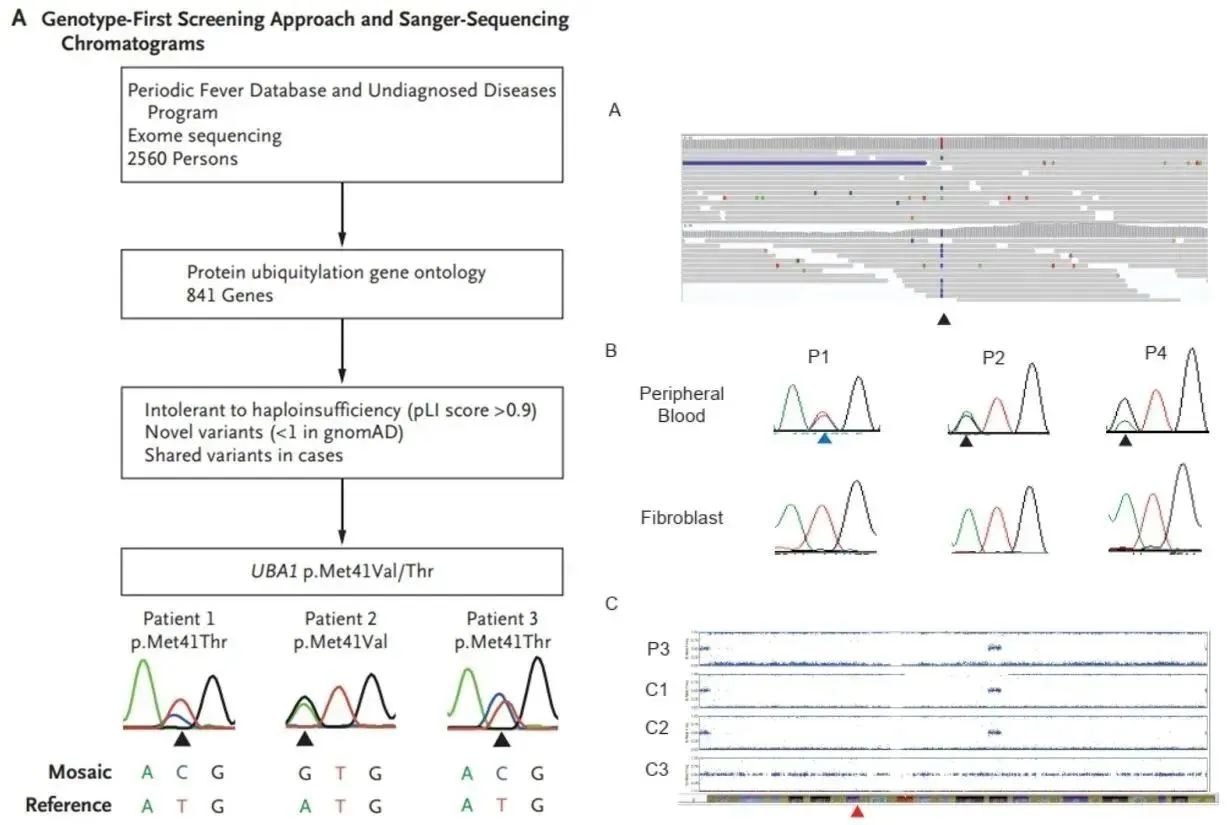
注:蓝色三角形:(c.122 T>C, p.Met41Thr)
黑色三角形:(c.121 A>G, p.Met41Val)
分离并测序了患者的不同的造血细胞群发现 ,患者的淋巴细胞(T和B细胞)中未检测到突变,呈现野生型,骨髓细胞(中性粒细胞和单核细胞)中检测到UBA1嵌合突变。因此,UBA1嵌合变异体是在祖细胞和髓系细胞中富集,而在成熟淋巴细胞中未发现该变异。
在NIH临床中心的观察队列中,确定了另外22名具有重叠临床表型的参与者:复发性多软骨炎患者队列、基于其临床特征(患有成人发病炎症综合征和血细胞减少症,以及软骨炎、血管炎、嗜中性皮肤病或其组合的男性)的基因筛查的参与者。
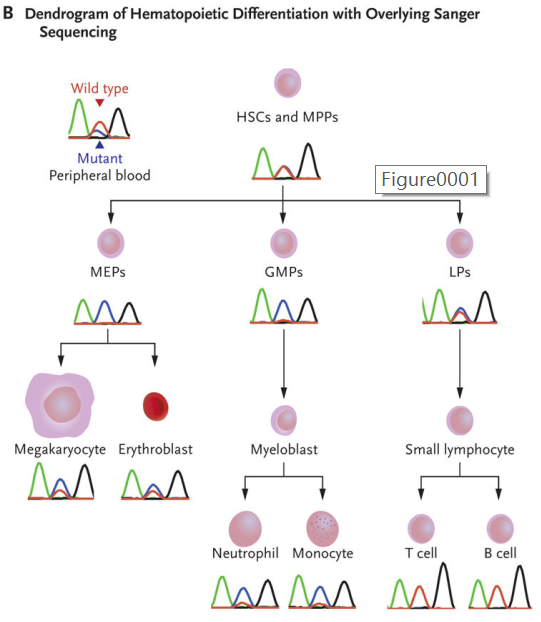
病例的分选的骨髓祖细胞和外周血谱系的造血分化的树状图
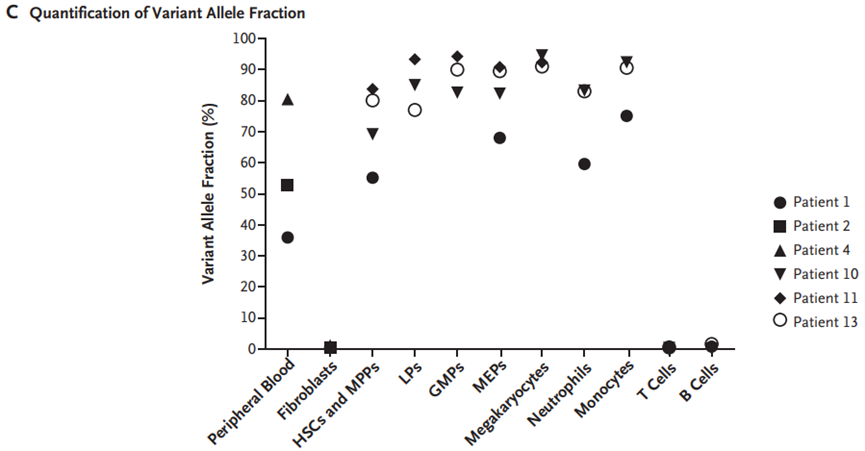
在分离的细胞系中使用数字液滴聚合酶链式反应分析对变异等位基因分数的定量
03
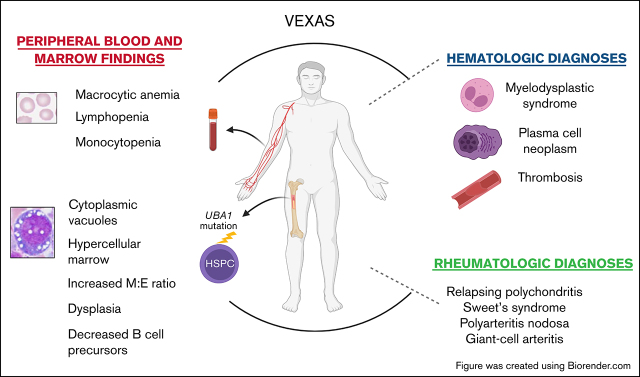
VEXAS综合征的临床特征
在这些患者中,通常会在成年后期出现致命的、治疗难治性炎症综合征,伴有发热、血细胞减少、骨髓和红系前体细胞中的特征性空泡、发育不良的骨髓、中性粒细胞皮肤和肺部炎症、软骨炎和血管炎。
这 25 名患者中的大多数符合炎症综合征(复发性多软骨炎、Sweet 综合征、结节性多动脉炎或巨细胞动脉炎)或血液系统疾病(骨髓增生异常综合征或多发性骨髓瘤)或两者兼有的临床标准。
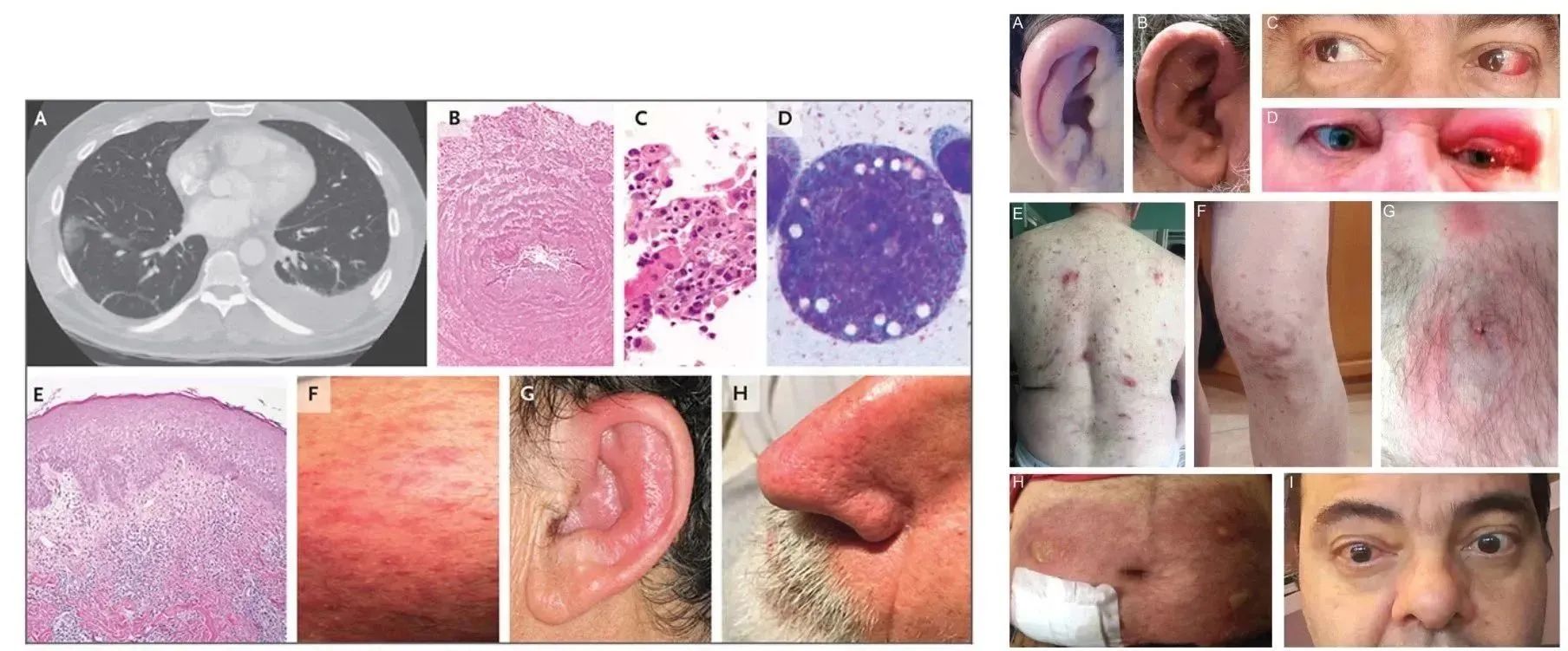
04
VEXAS综合征和细胞质缺失UBA1 功能
UBA1编码所有细胞泛素信号启动所需的主要E1激活酶。UBA1表达为翻译起始位点不同的两种同工型——细胞核UBA1a(起始于p.Met1)和细胞质UBA1b(起始于p.Met41)。
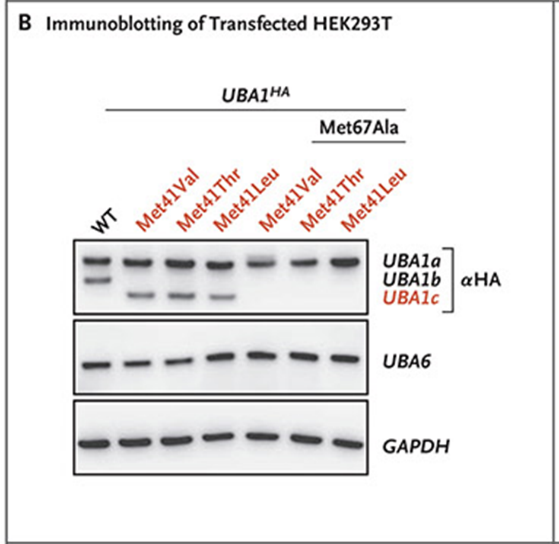
影响 p.Met41 的突变导致UBA1 的典型细胞质转录本丢失,并导致在 p.Met67 开始的新型催化受损转录本的表达。血凝素(HA)标记的UBA1 Met41构建体导致一种新的短同工型的表达,Met67Ala突变的引入消除了这种表达。引入以Met67密码子为目标的突变导致了快速迁移带的消失,这表明UBA1的这种新亚型的信使RNA的转录(此处记为UBA1c)是从Met67密码子开始的。
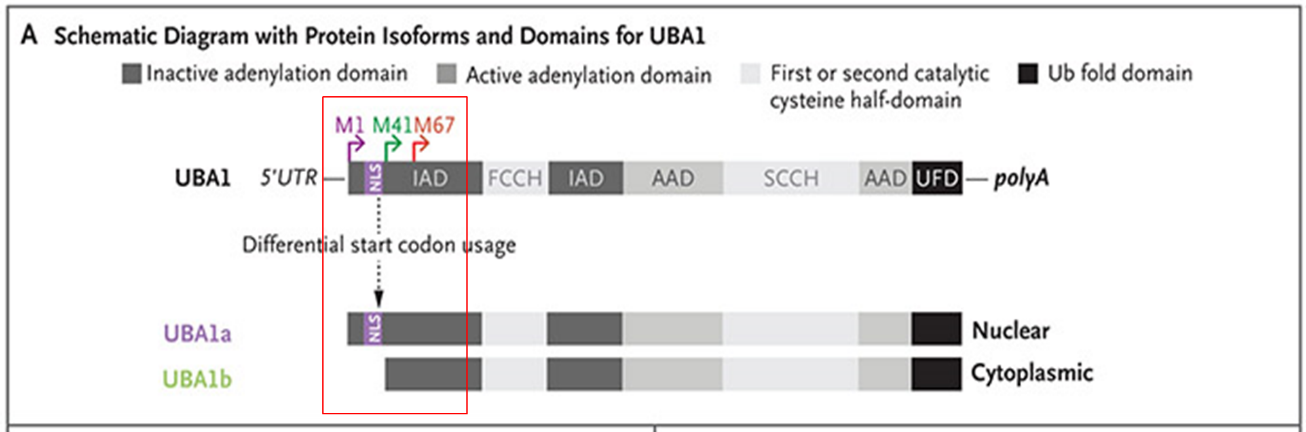
通过免疫印迹分析了UBA1 Met41变异体在人胚胎肾(HEK293T)细胞中的表达,结果显示UBA1b的丢失,同时产生了一个未预料到的快速迁移带UBA1c,这个快速迁移带的蛋白质可能是由于下游产生了新的起始密码子。
斑马鱼uba1和人类UBA1高度同源。因为uba1对生存能力至关重要,作者通过CRISPR-Cas9编辑的斑马鱼模型评估了早期发育过程中的炎症。
UBA1是几乎所有细胞泛素信号传导所必需的,在模式生物和培养细胞中是必不可少的。UBA1变异只存在于体细胞状态,这可能反映了影响p.Met41的突变在生殖细胞中是致命的,而这种突变只有在特定细胞类型中镶嵌时才与生命相容。
1. 缺乏uba1的斑马鱼系在受精后7-21天内也表现出生长异常和死亡,与在VEXAS综合征参与者中发现的体细胞变异相比,可能部分归因于这些突变的生殖细胞性质。
2. 与Δuba1a和对照组相比,Δuba1或Δuba1b,导致了斑马鱼炎症基因表达的上调;受精后4天的胚胎中导致中性粒细胞数量减少。
3. 敲除斑马鱼细胞质uba1引起全身炎症。
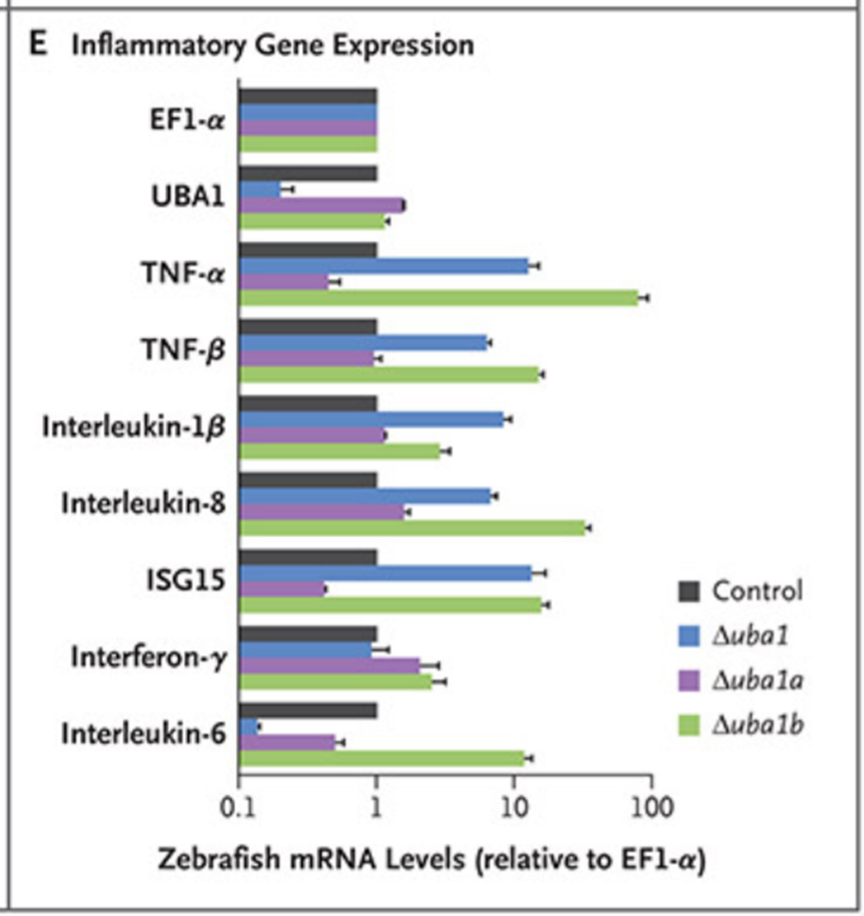
斑马鱼uba1基因敲除系胚胎的炎症基因表达水平
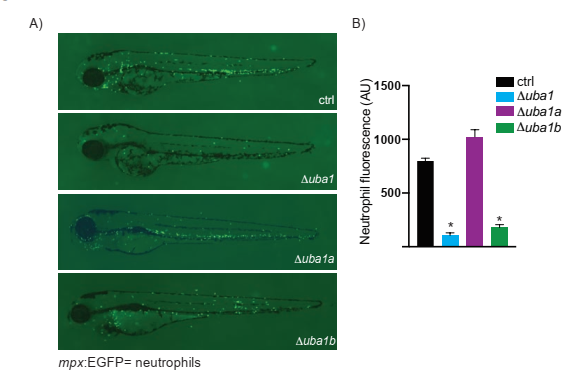
斑马鱼uba1基因敲除系的中性粒细胞分析
1. Δuba1是通过引入M67下游的移码突变(c.455_458del, p.T512M, fs*2)而产生的,导致转录本表达减少,很可能是由无意义介导的mRNA衰变所致;
2. Δuba1a是通过在M1和M41 (c.53_56del, p.S15Ifs*29)之间引入移码突变产生的,有利于在M41起始和Uba1b亚型的翻译;
3. Δuba1b是通过引入M41位点的缺失而生成的(c.118_123del, p.G40_M41del),导致uba1b的丢失,可能有利于M67位点的起始和Uba1c亚型的转译。
05
不同变异形式与表型关联性
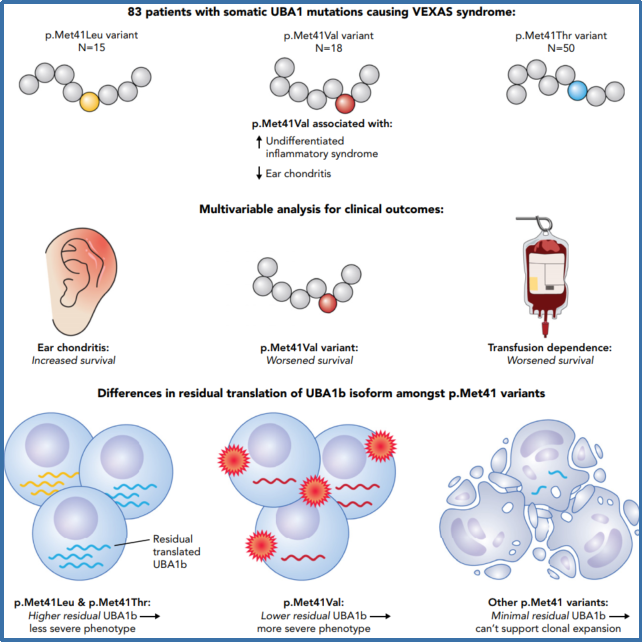
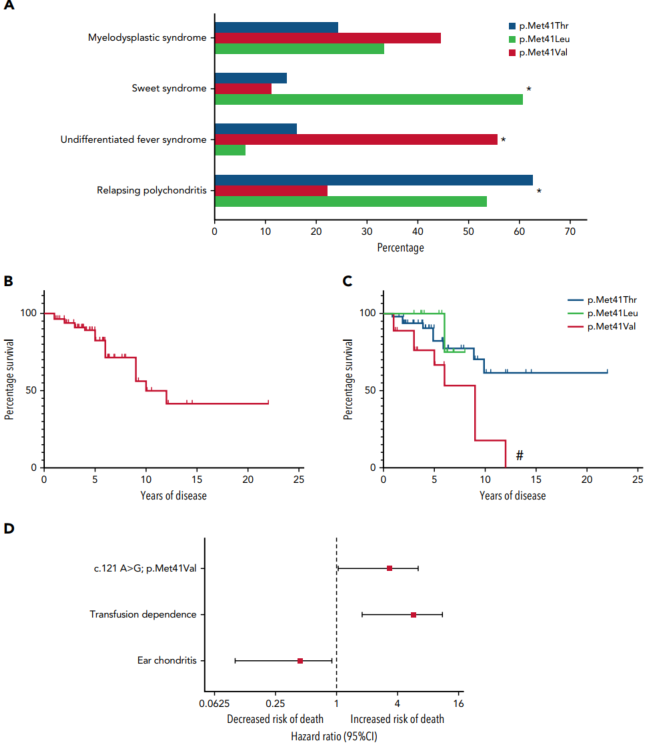
Ferrada等人证明了由三种典型UBA1突变(p.Met41Val)中的一种引起的空泡、E1 -酶、x连锁、自身炎症、体细胞综合征(VEXAS)的患者有更多的全身炎症综合征,生存率更差,正常细胞质UBA1亚型UBA1b的残留翻译更低。这将VEXAS的发病机制和严重程度与UBA1b功能的丧失联系起来。
带有p.Met41Val变异的VEXAS患者有更多的全身无分化炎症综合征和较少的耳软骨炎。生存的多变量分析显示,耳软骨炎患者预后改善,输血依赖或p.Met41Val变异患者预后较差。p.Met41Leu和p.Met41Thr变异有较高的正常细胞质UBA1 (UBA1b)残留翻译,而p.Met41Val的UBA1b残留翻译较低,p.Met41的其他排列有最低的UBA1b残留翻译。
06
VEXAS综合征的患者生存分析
Met41Val基因型和输血是血液学表现的重叠。VEXAS综合征的特点是风险死亡率的高度依赖性和显著的临床异质性。
分析了83例UBA1体细胞致病性变异在p.Met41位点 (p.Met41Leu/Thr/Val)的患者,UBA1细胞质亚型翻译的起始密码子(UBA1b)。p.Met41Val基因型患者在疾病分化性炎症综合征中最有可能存在差异。多因素分析显示,VEXAS综合征的耳软骨炎严重程度与生存率增加相关,而输血依赖和p.Met41Val的残留翻译变异与生存率降低独立相关。
07
VEXAS综合征疾病分子诊断
目前由于VEXAS综合征患者自身炎症症状出现的时间比血液学症状要早得多,血液系统不一定是首发表现,可能部分患者首诊在风湿免疫科,由于部分医生对该病的认识不够,加上UBA1基因并没有纳入常规的NGS检测中,在临床有可能会漏诊该病。
形态学上出现多系细胞,尤其是髓系和红系前体细胞胞浆空泡,可考虑该病的可能,再结合临床表现提示临床医生进行UBA1基因的突变检测,才能增加该类疾病的检出率。
在基因时代,骨髓细胞形态学仍然具有不可替代的地位,在形态学的基础上结合ICM检查,才能更好地做出精准诊断、精准治疗。
分子诊断:UBA1突变仅限于髓系细胞,血液的体细胞突变。
送检类型
测序先证者血液+皮肤组织(验证)
(UBA1突变仅限于髓系细胞,血液的体细胞突变,中性粒细胞性皮肤病患者皮肤组织)
08
案例分享
受检者信息:男,临床怀疑VEXAS综合征
检测策略:临床全外显子测序(含线粒体) 血液+组织送检
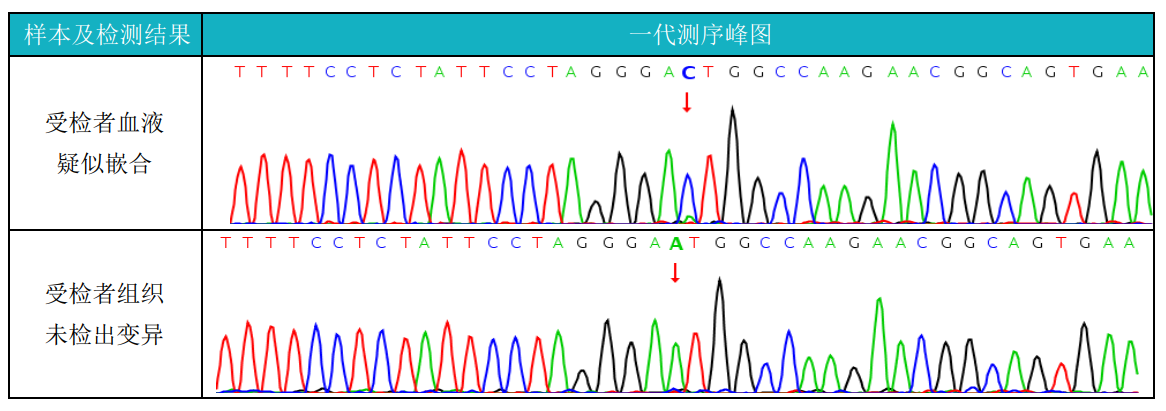
检测结果:发现受检者血液样本中检出 UBA1 基因上的一个疑似嵌合错义变异,一代测序验证结果显示该变异真实可靠,受检者组织样本中未检出该变异。UBA1 基因体细胞变异可导致 VEXAS 综合征(OMIM#301054)等疾病。
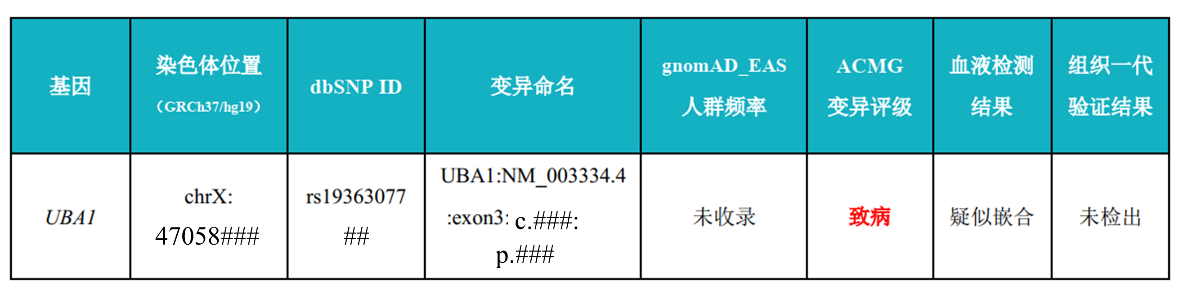
血液和组织的一代验证: